- 엄태선 기자/ 승인 2025.04.14 05:53
약사법에 따라 희귀약 10년(소아적응증 추가시 1년 연장), 신약 6년의 의약품 자료보호를 받지만 그외 자료보호를 받는 사례는 무엇일까.
식약처는 11일 2025년 상반기 의약품 허가심사 설명회를 통해 이같은 유형사례를 공유했다.
희귀약과 신약 외 유효성분 종류 등 중요사항 변경하는 의약품의 경우 허가 당시 개별성분의 병용요법을 입증하기 위해 제출한 임상시험자료는 6년이 부여된다.
예를 들어 고혈압치료제로 개별 단일제(A, B) 품목의 허가사항에 각 단일제와의 병용요법이 기재되지 않아 허가신청시 임상시험자료를 제출한 복합제의 경우다.
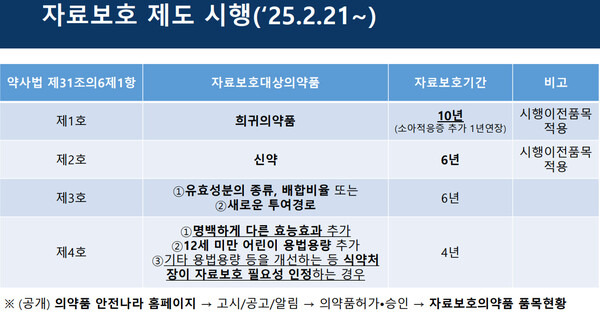
또 이미 허가된 의약품과 유효성분은 동일하나 투여경로나 다른 전문약으로 허가 당시 제출한 임상시험자료는 자료보호기간 6년이 부여된다. 예를 들어 레바미피드(경구제→점안제), 도네페질(경구제→경피흡수제) 등이 이런 사례다.
이밖에 새로운 환자군에 적용되는 명백하게 다른 적응증 추가시 제출한 임상시험자료는 4년이 부여된다. 피나스테리드, 두테스테리드 제제가 전립성비대증서 탈모치료제로 확대된 경우다.
여기에 12세 미만 어린이 용법용량을 허가받은 의약품이 허가시 제출한 어린이 대상 임상시험자료는 4년이 부여되며, 식약처장이 자료보호가 필요하다고 인정한 용법용량 개선, 효능효과 추가 등 품목별로 검토해 임상시험자료 4년 부여하게 될 예정이다.
다만 자료보호의약품의 임상시험자료를 인용 또는 원용하고 새로운 임상시험자료를 제출하지 않은 의약품은 자료보호대상이 아니며 임상시험 동의서 제출해 허가신청한 품목은 주관사 품목만 자료보호기간을 부여하고 공개하게 된다.
http://www.newsthevoice.com/news/articleView.html?idxno=41855
'오늘의 제약뉴스' 카테고리의 다른 글
| 증가세 '콜린제제' 관리방안...건보공단의 핵심포인트는? (0) | 2025.04.16 |
|---|---|
| 그래프로 보는 제약기업 지난 10년 성적표(64)...에이프로젠바이오로직스 (0) | 2025.04.14 |
| 올해 추진 의약품 안전성-유효성 지침-가이드라인은 '이것' (0) | 2025.04.14 |
| 당뇨병-이상지질혈증 환자 1194명 대상 시판후 조사 결과는? (0) | 2025.04.11 |
| '세나진정' 등 생산지연-중단-선적지연 등 공급불안정 (0) | 2025.04.11 |
