- 엄태선 기자
- 승인 2022.04.13 06:09

5년마다 의약품 제형별로 생산시설에 대한 적합성을 평가받아 국가가 인정해 주는 GMP 적합판정서를 발급받은 업체는 얼마나 될까.
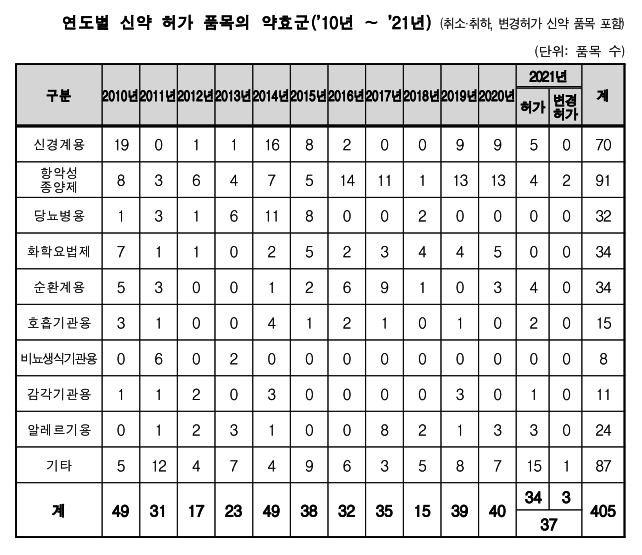
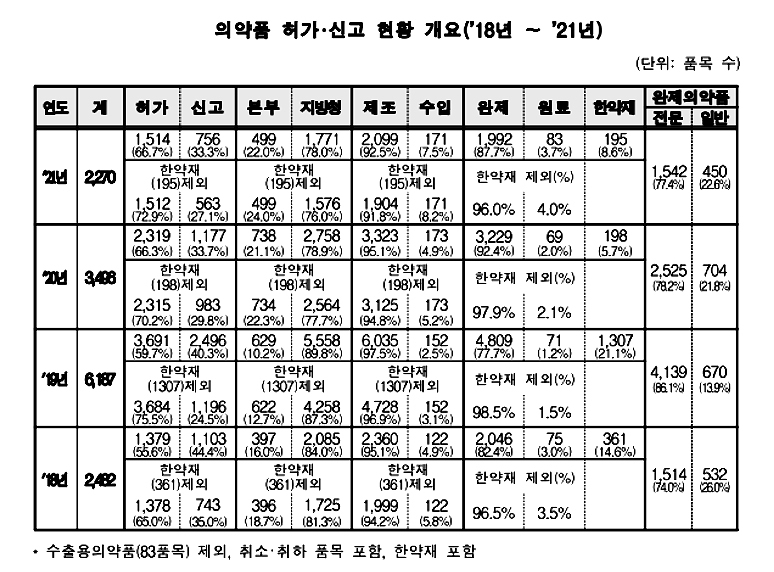
12일 기준 식약처의 의약품GMP적합판정서 발급 현황에 따르면 국내 소재 의약품 제조로 인정된 GMP시설은 총 552건에 달하는 것으로 나타났다. 발급된 적합판성서 중 완제의약품은 405건, 원료의약품은 147건이었다. 업체는 400여곳에 달한다.
업체별로는 에이치케이이노엔과 녹십자, 신풍제약이 각 완제의약품 3건, 원료의약품 2건 등 5건이었으며 방사성의약품을 생산하는 듀켐바이오가 5건을 가장 많았다.
이어 한미약품과 동국제약, 보령, 휴젤이 완제 2건-원료 2건이었며 종근당바이오가 완제 1건-원료 3건, 경방신약이 완제 3건-원료 1건으로 총 4건씩이었다. 또 디아이지에어가스와 단일가스켐, 에이치디엑스가 4건씩이었다.
이밖에 LG화학, 동아제약과 동아에스티, 대웅제약과 대웅바이오, 경동제약, 삼양홀딩스, 다산제약, 화일약품, 동방에프티엘, 유니메드, 코러스제약, 린데코리아, 에이프로덕츠코리아가 각 3건씩이었다.
제형별(중복)로는 내용고형제 160건, 주사제 117건, 특수제제 103건 합성(무균, 비무균) 66건, 가스군 51건, 외용액제 28건 등이었다.
한편 국내 제조시설을 철수하고 있는 다국적 제약사들도 일부 남아있었다. 일본제약사인 오츠카와 이스라엘 다국적 제네릭사인 알보젠이 각 2건이었다.
적합판정서 유효기한이 얼마남지 않은 제조소는 중헌제약의 청주 소재 시설이 오는 16일까지, 안트로젠의 서울 금천 25일, 경남제약의 경남 의령 5월1일, 동아제약의 충남 천안 5월1일, 명인제약의 경기 화성 5월2일, 에이치케이이노엔의 청주 층덕구 소재 제조소가 오는 5월2일까지이다.
의약품 GMP적합판정서, HK이노엔-녹십자 등 4곳 최다 - 뉴스더보이스헬스케어 (newsthevoice.com)
'오늘의 제약뉴스' 카테고리의 다른 글
| 대조약없이 이동시험, 사전검토로 심사?...민원궁금증들 (0) | 2022.04.15 |
|---|---|
| 의협 반대한 '한약제제 허가규정'...11일 식약처 개정고시 (0) | 2022.04.13 |
| 시판 후 안전관리 전담 조직-인력..."대규모 증원 필요" (0) | 2022.04.13 |
| 동국, 판시딜 등 캡슐제-프리필드 매출 폭증에 '함박웃음' (0) | 2022.04.12 |
| HK이노엔-종근당바이오-녹십자, 임상시험 불붙었다 (0) | 2022.04.12 |