- 엄태선 기자
- 승인 2022.03.24 07:15

국내외 제약사가 공급하는 의약품들이 잇따라 품절되는 한편 회수 및 생산중단을 이어가고 있다.
23일 유통업계에 따르면 화이자제약을 비롯해 한국파비스제약, 영일제약, 제일약품, 보령제약 등이 품절 또는 생산중단되는 품목을 거래처에 안내했다. 원료수급 및 생산지연 등의 원인이 대부분이다.
먼저 한국화이자제약의 경우 혈우병치료제 '베네픽스주'와 항생제 '타조신주'가 품절됐다.
화이자제약은 '네네픽스주 250IU/Vial' 제형의 제조원 생산일정 지연으로 인해 품절됐으며 재공급은 오는 28일 마지막주로 예상된다고 밝혔다.
또 '타조신주4.5g 10V' 제형도 제조사의 행정처분으로 인한 제품 지연으로 품절이 예상되며 장상적인 공급은 오는 4월초순에 가능할 것으로 예상했다.
한국파비스제약은 항히스타민제 '베타틴정' 30T와 300T 모두 품절됐으며 오는 4월 중에 공급이 재개될 것이라고 알렸다.
또 영일제약은 전문약인 향정감기약 '코프론정'과 일반 감기약 '포린정'이 원료수급 문제로 생산을 중단했다고 전했다.
제일약품도 피해 갈 수 없었다. 대표브랜드인 '케펜텍'에 대한 공급 차질을 알렸다. 붙이는 소염진통제 '케펜텍 엘 플라스타 7매'와 '케펜텍 플라스타(보) 6매'가 원부자재수급 지연과 생산라인 개선의 이유로 생산지연돼 품절된 상태인 것. 케펜텍 엘 플라스타는 오는 5월 중순에, 보험용인 케펜텍 플라스타는 오는 28일경 공급이 이뤄질 예정이다.
보령제약은 항생제 '보령답토마이신주350mg'과 '보령답토마이신주500mg'을 유효기간 만료 후 공급중단을 결정했다고 전했다. 350mg은 오는 10월4일, 500mg은 내년 2월14일까지이다.
또 보령제약은 비염약' 리노에바스텔캡슐'300C와 30C가 현재 재고가 없다며 오는 4월8일 유통이 가능한 실정이라고 밝혔다. 이번 품절은 주원료 수급과 QC 지연으로 입고가 연기된 것이다.
한편 명인제약은 치매약 '리셀톤패취'과 관련해 아이큐어에서 전공정 생산중 안정성시험에서 일부 제조번호에서 유연물질 기준이 초과됨에 따라 현재 회수 중이라고 밝혔으며 팜젠사이언스은 소화성궤양치료제 '네이자틴캡슐'이 NDMA 검출로 인해 자진회수 중이라고 전했다.
제약 품절-생산중단 줄이어...일정지연-원료수급 원인 - 뉴스더보이스헬스케어 (newsthevoice.com)
'오늘의 제약뉴스' 카테고리의 다른 글
| 올리고핵산치료제 CDMO로 글로벌 1위 도전 에스티팜 (0) | 2022.03.28 |
|---|---|
| 휴온스-광동-대웅-종근당, 생산공장 110%이상 '풀가동' (0) | 2022.03.28 |
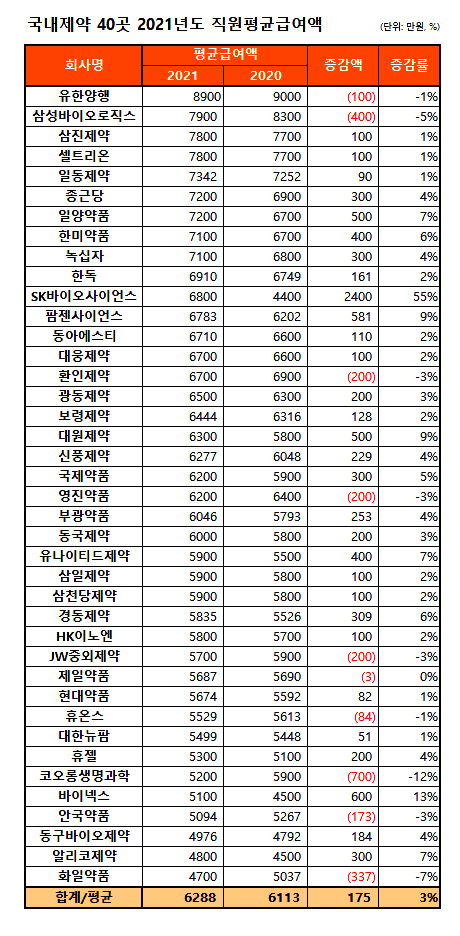
| 국내제약 40곳중 최고 연봉은 어디?...여전히 유한양행 '우뚝' (0) | 2022.03.24 |
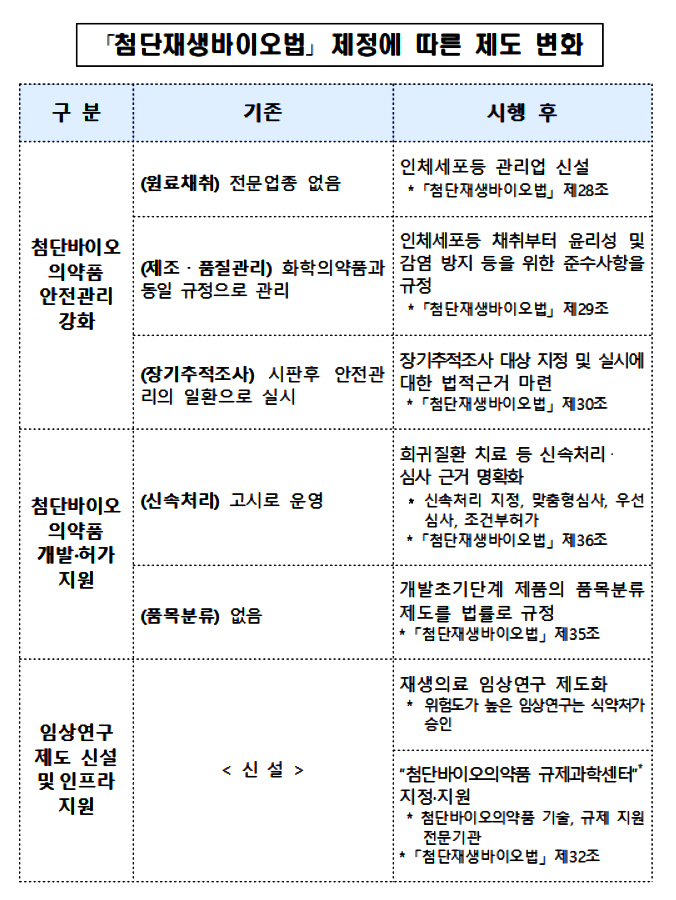
| 첨단재생바이오법 제정 이후 제도변화는 어떻게? (0) | 2022.03.24 |
| 대조약 관리 식약처 담당자 1명...쏟아지는 신청 '감당안돼' (0) | 2022.03.23 |