- 엄태선 기자/ 승인 2024.03.04 06:28

식약처에 등록된 의약품등의 해외제조소가 지난 2월말 기준 1만832건에 달하는 가운데 해외제조소에 대한 보다 효과적인 현지실사를 위해 올해부터 그 수를 대폭 확대한다.
식약처는 지난해 의약품등 해외제조소 등록제 정착과 등록 대상 확대로 의약품 해외제조소 안전관리 기반을 강화해왔다.
자사제조용 원료의약품을 등록대상으로 확대하는 내용의 약사법이 2021년 7월20일 개정돼 본격적으로 2022년 7월22일 시행돼 전면 의무화됐다.
이에 2022년에 이어 2023년 연간 50개소에 대한 현지실사를 추진해왔으나 올해부터는 실사를 2배 확대한 100곳에 대해 진행할 것을 목표하고 있다. 이같은 확대돈 실사를 위해 예산도 지난해 4억9700만원에서 올해 9억9400만원을 확보한 바 있다.
실사는 상반기 대상 위험도 평가를 지난해 11월에 끝내 올 1월부터 50곳에 대한 실사에 들어갔으며 하반기 살사대상 위험도 평가는 오는 4월에 마무리해 7월부터 들어갈 예정이다.
다만 실사 대상 확대에 따른 인력확보 상황을 고려해 비대면 실사 등 다양한 실사방식을 적용해 효율적으로 운영할 방침이다.
GMP현장감시, 무통보 불시점검 실시
정기감시, 제형당 5품목서 3품목으로 조정
특별기획감시, 중점점검 필요항목 한정 점검
한편 식약처는 위험도 상위 등 의약품 GMP 제조소 현장감시의 경우 정기약사감시 대상 위험도 상위 제조소 및 특별기획감시 대상에 대해 무통보점검(불시점검)을 실시해 감시 효율성을 높일 예정이다.
약사감시도 현행 업체 전반에 대한 점검방식에서 제조소별 중점점검 사항으로 점검 방식 전환도 이뤄진다. 여기서 중점점검사항은 제조소의 위험도 평가결과, 점검 및 실사 이력, 회수 이력 등을 종합적으로 검토해 설정하고 해당 사항을 본부-지방청 약사감시 정보 공유방에 주기적으로 반영해 운영하게 된다.
뿐만 아니라 국내 제약업체의 GMP 적합 제형 보유 현황상 통상 3~4개임을 감안해 약사감시 대상 품목 수를 제형당 5품목서 3품목으로 조정, 약사감시 집중 환경을 조성할 방침이다.
다시말해 정기약사감시는 제형당 5품목서 3품목으로, 특별기획감시는 GMP전반에 대한 점검서 중점점검 필요 항목 한정 점검으로 개선한다.
의약품등 해외제조소 등록 1만832건...올해 현지실사 100곳 - 뉴스더보이스헬스케어 (newsthevoice.com)
'오늘의 제약뉴스' 카테고리의 다른 글
| 약의 빛과 그림자...유한양행(1) 안티푸라민-로수바미브정 (5) | 2024.03.05 |
|---|---|
| 국가출하승인제도 검정시료, 올해 세부운영안 마련 (1) | 2024.03.05 |
| 안전관리 신뢰성 위한 'GMP실태조사 공개' 법개정 '진행중' (0) | 2024.03.04 |
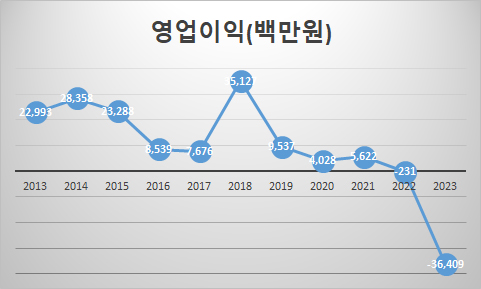
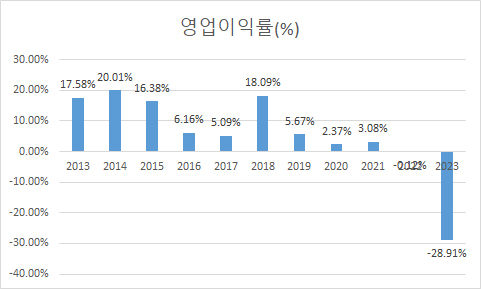
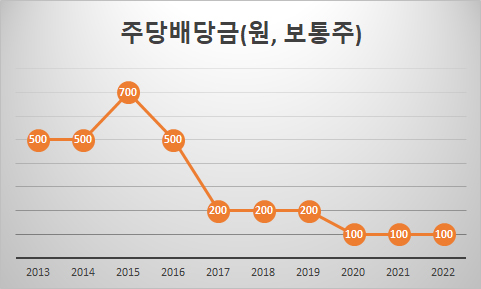
| 그래프로 보는 제약기업 지난 10년 성적표(28)...부광약품 (0) | 2024.02.28 |
| 허가시 임상자료 보호...신약 등 위해성관리 신설 (0) | 2024.02.27 |