주경준 기자/ 승인 2021.06.02 07:19
바이오시밀러 6품목 글로벌시장 경쟁...순차적 국내도입 검토
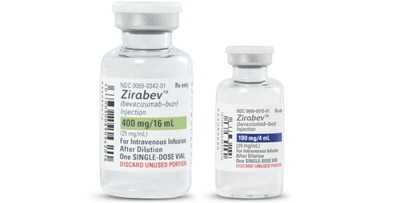
항상 제네릭의 공세에 방어전만 치루던 한국화이자가 도전자로 입장이 바뀌었다. 바이오시밀러 '자이라베브'(Zirabev)로 로슈의 아바스틴(베바시주맙) 아성에 도전한다.
1일 화이자는 바이오시밀러 항암제 '자이라베브주' 국내 허가 소식을 전했다. 국내 시장에서 처음으로 오리지널 타이틀 없이 도전자 입장에서 출시하는 첫 제품이다.
또 화이자가 글로벌시장에서 구축하고 있는 '바이오시밀러' 제품라이업을 고려할 때 '자이라베브주'는 화이자의 본격적인 바이오시밀러 국내시장 진출을 알리는 신호탄으로 업계는 분석하고 있다.
자이라베브주에 이어 언제든 국내도입이 가능한 바이오시밀러 품목은 항암제 트라지메라(Trazimera, 트라스투주맙), 룩시엔스(Rxience,리툭시맙) 등이 꼽힌다. 각각 허셉틴과 맙테라가 오리지널이다.
암환자의 호중구감소증 치료제 니베스팀(Nivestym, 필그라스팀)과 나이베프리아(Nyvepria페그필그라스팀)는 각각 뉴포젠과 뉴라스타를 타겟으로 출시된 바이오시밀러 라인업이다.
빈혈치로제 빈혈치료제 레타크리트(Retacrit, 에포에틴)도 있다. 또 휴미라(아달리무맙)의 바이오시밀러는 애브비와 합의에 따라 23년 미국시장에 출시할 예정이다.
이외 화이자는 셀트리온의 레미케이트 바이오시밀러 '램시마'를 미국시장에서 '인플렉스라'라는 상품명으로 판매하며 상당한 성과를 거두고 있다.
자이라베브주에 이어 국내시장에 도입 가능 제품이 6품목에 달하고 바이오시밀러 제품에 대한 우호적인 약가정책을 갖고 있는 국내시장 상황에 비춰, 지속적인 국내출시가 예상된다.
또 관심을 갖고 살펴볼 대목은 화이자의 약가전략. 지난해 초 자이라베브주를 미국시장에 출시하면서 '아바스틴 대비 23% 정도 저렴한 공격적인 약가를 책정했다. 미국시장의 도매가격은 100mg당 613.4달러로 해당 용량은 아바스틴 4ml 에 대응한다. 참고로 국내 아바스틴 해당 용량 약가는 33만 387원으로 미국약가 대비 절반 이하다.
화이자는 "지난17일 식약처 허가를 받아 약가를 논하기는 이른 시점이나 글로벌시장과 동일하게 환자의 접근성을 높일 수 있는 합리적 약가를 책정하기 위해 노력할 계획" 이라고 밝혔다. 자이라베브주는 당장 삼성바이오에피스가 허가받아 보령제약이 판매하는 온베브지주와 함께 경쟁해야 한다.
한편 업계는 자이라베브주가 국내 바이오시밀러 시장경쟁에 글로벌제약사들이 본격적으로 합류하는 촉매 역할을 할 것으로 진단했다.
http://www.newsthevoice.com/news/articleView.html?idxno=20002
'다양한 보건의료뉴스' 카테고리의 다른 글
| '골참육단' 급여편향성 지적...골절예방 2025 로드맵 제안 (0) | 2021.06.04 |
|---|---|
| 이영희 약가제도기획부장 1급 승진...7월 실장직위 발령 (0) | 2021.06.02 |
| 콜린 약품비 환수협상 후속조치, '재협상명령'으로 가닥 (0) | 2021.06.02 |
| 6월에 신설되거나 바뀌는 약제 급여기준은? (0) | 2021.06.01 |
| 국가필수약 심평원 삭감?...병원 삭감사례 조사 (0) | 2021.06.01 |