- 엄태선 기자/ 승인 2025.06.27 05:54
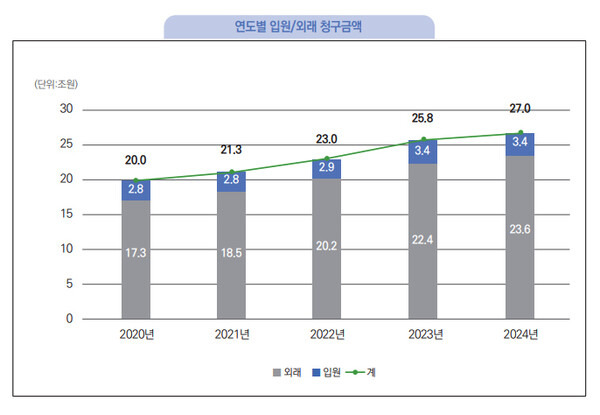
지난해 완제의약품 공급액 중 도매가 차지하는 비중이 55.8%에 달하는 것으로 나타났다. 또 전체 4117개소가 100조4552억원을 공급했으며, 업체당 평균은 244억원이었다.
건강보험심사평가원의 '2024 완제의약품 유통정보 통계집'에 따르면 지난해 전체 완제약 공급금액 중 도매상이 56조87억원을 공급해 이와 같았다. 이는 3678개소가 공급한 액수이며, 업체당 평균 153억원이었다.

제조사는 279개소가 33조2655억원을 공급해 평균 1192억원에 달했다. 전체의 33.1%의 비중을 기록했다. 수입사는 160개소가 11조1810억원을 공급해 평균 699억원이었으며, 11.1% 비중을 보였다.
특히 상위 5% 공급업체만을 볼때 전체 업체수는 206곳이 완제약을 공급했으며 73조5456억원을 찍어 전체의 73%를 차지했다. 반대로 상위 5%를 제외한 95%가 불과 27%를 나눠 공급했다.
업태별로는 도매 93개소가 35조4841억원을 공급해 평균 3815억원이었다. 공급액 점유율은 63%로 전체 점유율에 비해 낮았다.
제조사는 87개소가 28조9900억원을 공급해 평균 3332억원을 기록했다. 점유율은 87%로 매우 높았다. 수입사는 26개소가 9조715억원을 공급해 평균 3489억원에 달했다. 점유율은 81%였다.
제조-수입사, 요양기관 직거래 3.5조원...약국 공급 중 일반약 65.2% 차지
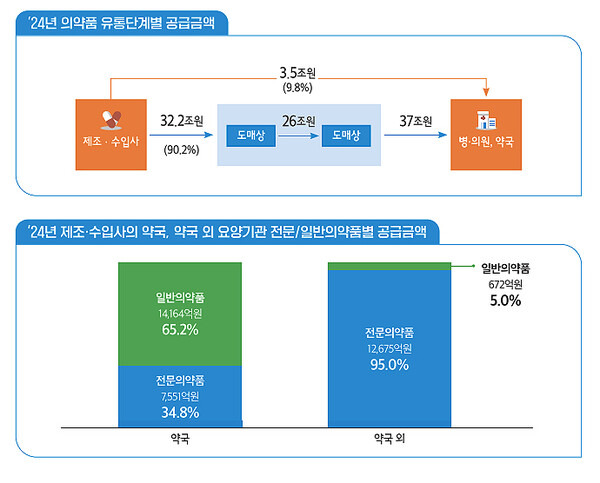
한편 제조-수입사가 공급하는 35조7000억원 중 요양기관에 직접 공급하는 비율은 9.8%, 3조5000억원이었다.
이중 약국에는 2조2000억원으로 전체의 62.9%, 그외 요양기관은 1조3000억원으로 37.1%였다. 약국에 공급된 의약품 중 전문약은 7551억원으로 34.8%, 일반약은 1조4164억원으로 65.2%로 일반약이 상대적으로 높았다. 이는 일반약의 경우 처방과 관계없이 약국에서 직접 판매가 가능하기 때문인 것으로 보인다.
약국 이외 요양기관에는 전문약이 1조2675억원으로 95.0%, 일반약은 672억원으로 5%에 불과했다.
http://www.newsthevoice.com/news/articleView.html?idxno=42674
'오늘의 제약뉴스' 카테고리의 다른 글
| 안전상비약, 지난해 555억원 공급...타이레놀·판콜·판피린 순 (0) | 2025.06.30 |
|---|---|
| 협상약제 이행관리 특이사항 신고...'이럴 때' 건보공단에 알려야 (1) | 2025.06.16 |
| 위험분담계약 약제, 제약의 이행...'곳곳에 빨간불 켜진다' (4) | 2025.06.12 |
| 애브비 '엡킨리주' 급여 한발짝...얀센 '텍베일리주' 벽에 (0) | 2025.06.12 |
| 10만원 이하 소액 처방거래처 해지..."치과는 정산해달라" 요청 (2) | 2025.06.12 |