문윤희 기자/ 승인 2021.09.24 06:16
합성신약 599개·바이오신약 540개·생물학적제제 376개 순
라이센스 비중 여전히 다국적사 집중…기업간 거래도 활발
올해 제약·바이오기업과 바이오벤처 등 국내에서 개발 중인 신약 연구 수가 1477건에 달하는 것으로 집계됐다.
이는 2018년 개발 중이었던 573건에 비해 무려 2배 이상 증가한 수치다.
이 같은 결과는 한국제약바이오협회가 지난 16일 발행한 '글로벌 제약강국을 위한 한국 제약바이오 파이프라인 조사 보고서'를 통해 나타났다.
이번 조사에 참여한 기업은 299곳이었으며 이 중 193개사가 연구를 진행 중이라고 답했다. 299개 기업 중 상장기업은 116개사가 포함됐으며 이들 회사의 R&D 투자 비중은 10.7%를 나타냈다.
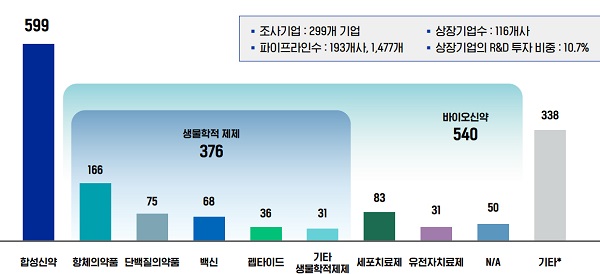
연구 중인 파이프라인에서 합성신약 개발 건수는 599개에 달해 최대 비중을 보였고 뒤를 이어 세포치료제와 유전자치료제를 포함한 바이오신약이 540개를, 항체의약품과 단백질의약품, 백신 등이 포함된 생물학적 제제 영역은 는 376개에 달하는 것으로 집계됐다.
천연물의약품과 융복합물질과 코드화 등 분류가 어려운 후보물질 등 기타 부분 파이프라인도 338개에 달했다.
임상단계별 파이프라인을 살펴보면 선도·후보물질 개발이 403건으로 전체의 27.3%대 비중을 보였고, 비임상이 397건으로 26.9%, 임상 1상이 266건을 보여 전체 18%를 차지했다.
임상 2상과 3상은 각각 169건과 116건을 보이며 전체 비중의 11.4%, 7.9%를 차지했다.
적응증별로 살펴보면 암이 최다 비중을 보였다. 암은 317건이 연구를 진행하며 전체의 21.5%를 차지했다.
뒤를이어 대사질환이 173건으로 11.7%대 비중을 보였고, 신경계통이 146건으로 9.9%, 감염성질환이 112건으로 7.6%대 비중을 보였다.
이밖에도 소화계통과 안구질환, 근골격계통, 순환계통, 피부질환과 호흡계통, 희귀질환, 비뇨생식계통이 10%대 이하의 비중을 차지하며 질환영역 별 연구 순위를 이어갔다.
항암제 파이프라인을 좀 더 세부적으로 살펴보면 총 317건 중 고형암 개발 비중이 138건으로 가장 높았다. 뒤를 이어 유방암이 39건, 혈액암이 18건의 순을 보였다.
임상 단계별 항암제 파이프라인 현황을 살펴보면 선도 및 후보 물질이 125건으로 가장 높았고, 비임상이 98건, 임상 1상이 51건, 임상 2상이 2건, 임상 3상이 10건에 달했다.
대형제약 중심 합성신약 개발 여전
국내에서 개발되는 합성 신약의 비중은 제네릭 출시 비중이 높은 대형제약과 중견제약에서 단연 높게 나타났다.
합성신약 파이프라인 연구 보유 수를 기업 규모별로 나눠봤을 때 대·중견기업이 375건을 보여 중소벤처사의 224건을 100건 이상 앞선 것으로 나타났다.
반면 바이오신약 부분과 천연물의약품 등 바이오신약과 기타 부분은 바이오번체 등 중소기업들이 우세한 비중을 보였다.
바이오신약은 399건이 중소벤처사에서 연구개발 중이었고, 기타 부분 역시 213건이 중소벤처사가 연구 중인 것으로 나타났다.
대중견기업의 바이오신약과 기타 부분 연구 건수는 각각 141건과 125건에 그쳤다.
자세한 내용은 아래를...
http://www.newsthevoice.com/news/articleView.html?idxno=22432
'오늘의 제약뉴스' 카테고리의 다른 글
| 격년제 약제 실거래가 조사 착수...내년 1월 약가인하 추진 (0) | 2021.09.27 |
|---|---|
| 유효기간 만료 도래...11월 갱신 신청품목 132품목 (0) | 2021.09.24 |
| 중국, 면역세포치료제 '중심'에 서다…美 추월 (0) | 2021.09.16 |
| “폐동맥고혈압치료, 초기 병용요법 요원" (0) | 2021.09.16 |
| 급부상 로슈, 황반변성 신약 2품목 올해내 FDA 승인결정 (0) | 2021.09.14 |


