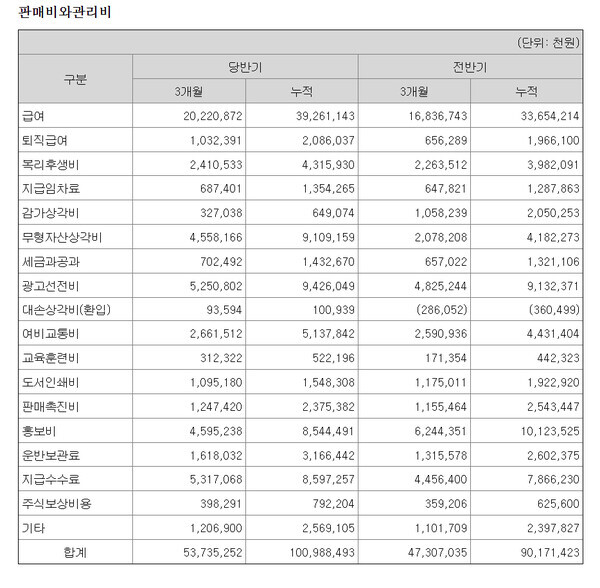
지난달 15일부터 9월27일까지 식약처 임상시험 승인 현황
국내외 제약사들이 소아질환부터 암질환까지 다양한 치료제 개발에 뛰어들었다.
식약처가 지난달 15일부터 27일까지 승인한 임상시험에 따르면 다국적 제약사의 경우 소아 희귀질환부터 항암제 개발에 주목하는 한편 국내제약사들은 소화질환부터 만성질환 치료제 개발에 관심을 보이고 있었다.
먼저 다국적제약사을 보면 사노피-아벤티스 코리아는 'SAR442501'에 대한 임상 2상을 추진한다. 소아 연골무형성증 시험대상자에서 피하 SAR442501의 안전성, 내약성, 약동학, 약력학, 유효성을 평가하기 위한 제2상, 공개, 다기관, 2단계 순차적 코호트, 용량 증량 국외개발 임상이다.
여기에 'SAR443765'에 대한 2상 국외개발 임상을 실시한다. 중등도 내지 중증 천식이 있는 성인 시험대상자를 대상으로 피하 SAR443765의 유효성, 안전성, 내약성을 평가하기 위한 임상이다. 연세대세브란스병원 등서 확인한다.
한국얀센은 'JNJ-77242113-AAC'에 대한 임상 3상을 진행한다. 중등증에서 중증의 판상 건선이 있는 임상시험대상자의 치료에서 무작위 배정 투여 중단과 재투여에 의해 JNJ-77242113의 유효성 및 안전성을 평가하기 위한 제3상, 다기관, 무작위 배정, 이중 눈가림, 위약 대조 임상시험 국외개발 임상이다. 서울아산병원 등 4곳서 진행한다.
여기에 'JNJ-77242113-AAC'에 대해 특정 영역에 이환된 판상 건선이 있는 임상시험대상자의 치료에서 유효성 및 안전성을 평가하기 위한 제 3상을 함께 실시한다. 분당서울대학교병원 등이 참여한다.
또 '사트랄리주맙(Satralizumab)'에 대한 국외개발 임상 3상도 함께 추진한다. 중등증 내지 중증 갑상선 안병증 시험대상자에서 사트랄리주맙의 유효성, 안전성, 약동학 및 약력학을 평가하는 제3상으로 중앙대병원 등 4곳서 그 가능성을 살핀다.
글락소스미스클라인은 '도스타리맙(Dostarlimab, GSK4057190)'에 대한 임상 2상을 실시한다. PD-L1 양성 재발성/전이성 두경부 편평세포암이 있는 시험대상자에서 마스터 임상시험계획서를 사용해 1차 치료로서 새로운 면역요법 병용을 평가하는 플랫폼 임상시험이다. 분당서울대병원 등 4곳에서 임상시험을 이끈다.
한국엠에스디는 'MK-1242(Vericiguat)정'에 대한 2/3상 국외개발 임상을 진행한다. 전신성 좌심실 수축 기능장애로 인한 심부전을 앓고 있는 소아 참가자를 대상으로 만성심부전 치료제 약 베리시구앗(vericiguat, 상품명 베르쿠보정)의 유효성과 안전성, 약동학을 평가하기 위한 임상시험이다. 양산부산대병원 등 4곳서 실시한다.
한국아스트라제네카는 'AZD5305'에 대한 임상 3상을 진행한다. 전이된 HRRm 및 비-HRRm 거세감수성 전립선암 환자를 대상으로 의사가 선택한 새 호르몬제제와 병용투여한 AZD5305 를 평가하는 무작위배정, 두 코호트, 이중 눈가림, 위약 대조 임상시험이다. 삼성서울병원 등 5곳서 실시시관을 맡았다.
베이진코리아는 'BGB-16673'에 대한 국외개발 임상 3상을 추진한다. B세포 악성종양 환자를 대상으로 한 브루톤 타이로신 키나아제 표적 단백질 분해제 BGB-16673의 용량증량 및 용량확장 임상시험이다. 서울아산병원 등 5곳서 실시한다.
아울러 'BGB-11417'에 대한 국외개발 1/2상도 함께 실시한다. 다발골수종에서 단독요법과 덱사메타손 및 카르필조밉과의 다양한 병용요법으로 투여하는 BGB-11417에 대한 시험이다. 서울대병원 등 5곳서 진행을 맡았다.
한국로슈는 '지레데스트란트(GDC-9545)'에 대한 국외개발 임상 3상을 시작한다. 이전 보조 내분비요법에 내성이 있는 에스트로겐 수용체 양성, HER2 음성 진행성 유방암 환자를 대상으로 CDK4/6 억제제와 병용 시 풀베스트란트와 비교한 지레데스트란트의 유효성 및 안전성을 평가하는 임상이다. 고려대병원 등 전국 10곳의 종합병원서 그 유효성 등을 살핀다.
여기에 트론티네맙(Trontinemab)'에 대한 임상 1/2상도 동시에 진행한다. 전조단계 또는 경증 내지 중등증 알츠하이머병 환자를 대상으로 RO7126209의 정맥 내 주입 후 안전성, 내약성, 약동학, 약력학을 연구하는 제1B/2A상, 무작위배정, 이중 눈가림, 위약 대조, 다중 상승 용량, 평행군 시험이다. 국외개발로 서울아산병원 등 3곳서 함께 추진한다.
한국비엠에스제약은 'BMS-986406'에 대한 임상 1상을 시작한다. 진행성 악성 종양이 있는 시험대상자를 대상으로 단독요법 및 병용요법으로서 BMS-986406의 제1상 최초 인체 적용 임상시험으로 서울대병원 등 4곳서 이를 확인한다.
이와함께 'BMS-986165(듀크라바시티닙)'에 대한 임상 3상도 진행한다. 활성 쇼그렌 증후군 시험대상자를 대상으로 듀크라바시티닙의 유효성 및 안전성을 평가하기 위한 임상시험으로 전남대병원 등 4곳이 실시한다.
한국화이자제약은 'PF-06823859'에 대한 임상 3상을 실시한다. 활성 특발성 염증성 근병증이 있는 시험대상자(활성 피부근육염 또는 다발근육염이 있는 시험대상자 포함)를 대상으로 PF-06823859의 유효성 및 안전성을 평가하기 위한 다기관 임상시험이다. 국외개발로 서울대병원 등 3곳서 맡는다.
국내제약사들도 치료제 개발을 위한 임상에 손을 놓지 않았다.
종근당은 당뇨 3제복합제 'CKD-379' 개발에 나섰다. 건강한 성인에서 음식물이 CKD379 의 약동학적 특성 및 안전성에 미치는 영향을 평가하기 위한 1상 임상시험으로 분당서울대병원서 실시한다. 여기에 'CKD-846'에 대한 건강한 성인 남성을 대상으로 후 약동학적 특성과 안전성을 평가하기 위한 임상 1상을 진행한다. 국내개발로 연세대세브란스병원서 진행한다.
종근당의 계열사인 경보제약도 'K08-22-18'과 'K08-22-19'에 대한 임상 1상을 에이치플러스양지병원서 진행한다.
에이치케이이노엔은 'IN-112420'에 대한 임상 1상을 추진한다. 건강한 성인을 대상으로 케이캡 주성분 '테고프라잔'과 항혈전제 성분인 '클로피도그렐' 병용 투여에 대한 임상 1상을 진행한다. 국내개발로 서울대병원에서 그 가능성을 살핀다.
한국유나이티드제약은 'UIC202304'과 'UIC202305'에 대한 임상 1상을 진행한다. 건강한 성인 자원자를 대상으로 UIC202304와 UIC202305의 병용 반복 투여 시 약동학적 상호작용, 안전성 및 내약성을 평가하기 위한 무작위배정, 공개, 2군, 2기, 반복투여, 임상시험이다. 메트로병원에서 이를 확인한다.
대웅제약은 'DWJ1622'에 대한 임상 1상을 진행한다. 건강한 성인 자원자를 대상으로 DWC202313 및 DWC202314 투여 시 안전성 및 약동학 상호작용을 평가하기 임상시험으로 에이치플러스양지병원에서 실시한다.
뿐만 아니라 항궤양제 'DWP14012정'에 대한 임상 3상도 함께 추진한다. 비미란성 위식도역류질환 환자를 대상으로 DWP14012의 유효성 및 안전성을 평가하기 위한 치료적 확증 임상시험이다. 국내개발로 한양대병원 등 전국 30곳에서 이를 확인한다.
이밖에도 젬백스앤카엘은 'GV1001'에 대한 2a상 국내개발 임상을 추진한다. GV1001-PSP-CL2-011 임상시험을 완료한 진행성 핵상 마비 환자를 대상으로 피하 투여 시 장기 안전성과 질환의 중증도 개선 효과와 안전성을 탐색하기 위한 12개월 연장시험이다. 서울대병원 등 5곳서 실시한다.
보령은 'BR1018'에 대한 임상 3상을 추진한다. 본태성 고혈압과 원발성 고콜레스테롤혈증을 동반한 환자를 대상으로 BR1018B와 BR1018C 병용 투여의 유효성 및 안전성을 비교 평가하기 위한 다기관, 무작위 배정, 이중 눈가림, 활성대조 임상시험이다.
한편 의료기관에서의 연구자 임상시험도 활발하다.
분당서울대병원은 'S-217622/오렌시아주'에 대한 연구에 착수했다. 입원한 코로나19 환자를 대상으로 아바타셉트 유효성 및 안전성 평가를 위한 다기관, 적응적, 무작위, 대조군 임상시험국외개발 임상을 진행하다. 서울아산병원 등 4곳서 진행한다.
또 전남대병원은 대웅의 '펙수클루정40밀리그램'에 대한 임상으로 클라리스로마이신 감수성이 있는 헬리코박터 파일로리균 제균 치료에서 펙수클루 기반 저용량 클라리스로마이신 삼제요법의 효용성 및 안정성에 대한 연구이다. 전남대병원 등 3곳서 진행한다.
삼성서울병원은 '레마로체주100mg'에 대한 국내개발 임상을 진행한다. 소아청소년 궤양성 대장염 환자를 대상으로 인플리시맙(Infliximab) 유도치료 기간중 유효성 및 안전성 평가를, 여기에 '파노린 주사(PANORIN)'에 대한 안면 골섬유이형성증 환자를 대상으로 정주 비스포스포네이트제 (Pamidronate disodium, 파노린 주사) 투여가 골용해성 병변의 성장속도 감소 및 골 통증 완화에 미치는 영향 연구자 임상시험도 함께 진행한다.
이외에 고려대구로병원은 '탁솔주(199604958)'에 대한 복막 전이를 동반한 진행성 또는 재발성 위암 및 위식도경계부암 환자를 대상으로 전신 항암요법과 함께한 복강 내 Paclitaxel 요법과 단독 전신 항암요법에 대한 3상 임상을, 연세대용인세브란스병원은 '펙수클루정40밀리그램'에 대한 내시경적 점막하 박리술 이후 발생하는 위궤양의 치료에서 펙수프라잔의 효과에 대한 연구자임상을 실시한다.